Gap-134 : une arme puissante contre la fibrose cardiaque

Mickaël Derangeon est maître de conférences et chercheur au sein du laboratoire de recherche de l’institut du thorax, dans l’équipe Ion Channels & Cardiac Arrhythmias. Il a obtenu un financement de la Fondation Genavie en 2014, puis en 2016. Il nous présente les découvertes de son groupe sur la fibrose cardiaque qui paraîtront dans Pharmacological Research en septembre 2020.
La conduction de l’électricité dans le cœur dépend de trois acteurs majeurs :
les cellules qui le composent,
le lien mécanique entre ces cellules appelé « matrice extracellulaire »
et la capacité du cœur à créer un courant électrique qui induira la contraction synchronisée de ce muscle.
En 1999, le laboratoire de recherche de l’institut du thorax a identifié pour la première fois une mutation dans le gène codant la protéine appelée Nav1.5.
Cette protéine produit l’électricité nécessaire à la contraction du cœur. La mutation identifiée provoque un mauvais fonctionnement de cette protéine Nav1.5, l’empêchant de créer un courant assez fort et rapide. Cela induit des troubles progressifs de la conduction cardiaque pouvant conduire à la mort subite du patient.
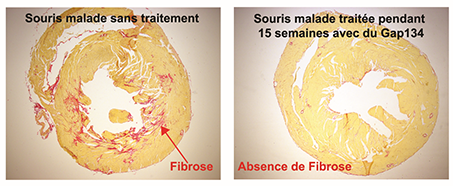
Ces troubles progressifs sont associés à l’installation d’une fibrose (en rouge ci-dessous). Cette fibrose correspond à une accumulation pathologique de matrice extracellulaire pouvant bloquer ou rendre difficile le passage du courant électrique dans certaine zone du cœur.
La fibrose est par conséquent un élément provoquant un risque majeur d’amplification et de création de troubles du rythme cardiaque pouvant être fatale pour le patient et commun à de nombreuses maladies cardiaques. Il est donc nécessaire de pouvoir inhiber la fibrose cardiaque afin de limiter les risques pour les patients.
Dans ce sens, une première étude financée par Genavie a été publiée par notre équipe en 2017. Elle nous a permis de comprendre que la Connexine 43 (Cx43), une protéine qui permet la communication entre les cellules du cœur, avait un rôle essentiel dans le mécanisme menant à ce processus délétère de la fibrose. De plus, grâce à cette étude, nous avons compris que le niveau d’expression de la Cx43 diminue fortement avec l’âge et qu’il pourrait s’agir du mécanisme expliquant l’établissement de la fibrose avec le vieillissement.
Dans cette optique nous avons essayé d’empêcher sur le cœur des souris l’établissement de la fibrose en augmentant l’activité de la Cx43 par une petite molécule testée dans des essais cliniques le Gap134. Comme le démontrent les photos, nous venons de mettre en évidence dans une nouvelle étude financée par Genavie que le Gap134 est un puissant inhibiteur de la fibrose cardiaque. Cette découverte ouvre de nombreuses perspectives puisque la Cx43 est aussi impliquée dans la fibrose de d’autres organes comme les poumons ou les reins.
Pour en savoir plus, lisez dès maintenant l’article à paraître dans Pharmacological Research : Gap-134, a Connexin43 activator, prevents age-related development of ventricular fibrosis in Scn5a+/− mice
Découvrez nos histoires de coeur : des projets scientifiques où le soutien de Genavie a joué un rôle clef :
Révolutionner la médecine en travaillant sur les cellules souches pluripotentes induites
Les cellules souches pluripotentes induites (Induced Pluripotent StemCells) sont des cellules obtenues à partir d’échantillons de peau ou d’urine, que l’on reprogramme pour les faire revenir à l’état de cellules souches pluripotentes, c’est-à-dire capables de former différents organes. Lire l’article

L’histoire des deux cousins ou quand nos spécificités régionales deviennent un outil de recherche biomédicale.
1996 – Deux patients hospitalisés dans le service de cardiologie de l’institut du thorax souffrent d’un prolapsus mitral. D’ordinaire, la valve mitrale impose un sens unique à la circulation du sang dans le cœur. Chez ces patients, cette valve fuit et entraîne une insuffisance cardiaque, maladie chronique très invalidante qui provoque, entre autres, une fatigue intense. Le prolapsus mitral touche 2% de la population mondiale. Son mécanisme est inconnu et il n’existe pas de prévention. Lire l’article